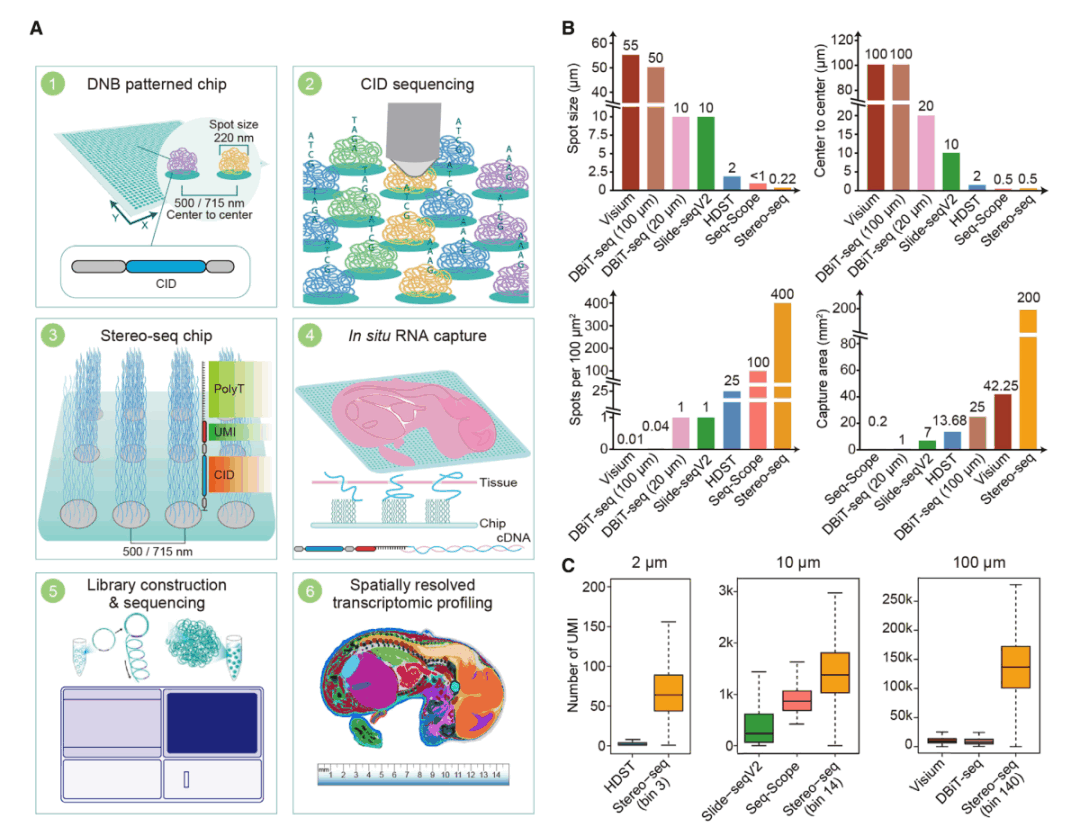
华大时空组学技术Stereo-seq是一项基于DNA纳米球测序芯片自主研发、可实现超高通量和超高精度的全景式时空转录组技术,它将认识生命空间的分辨率提升至500 nm的亚细胞层级,相比国际同类技术分辨率提升了40,000倍。Stereo-seq目前已被成功应用到动物胚胎发育、植物研究、脑科学、肿瘤等多个领域,并助力研究人员在Cell、Science、Nature、Cell Research等顶级学术期刊上发表了40余篇文章。
近日,华大时空组学STOmics与贝瑞基因达成合作,贝瑞基因正式成为华大时空组学STOmics生态合作伙伴。贝瑞基因在单细胞及空间转录组平台积累了丰富的服务经验,从各种组织的样本制备到生物信息数据挖掘,打造完善的售前售后服务体系,致力于为科研人员提供专业、前沿的科研服务。
此次贝瑞基因全面引进华大时空组学技术,将为研究人员提供更高精度的空转检测服务,助力广大科研工作者在生命结构、疾病机制、生长发育机制等研究领域获得新的认知。

01 纳米级分辨率,实现亚细胞级分子定位
Stereo-seq的检测分辨率可达到500 nm,能实现对单个细胞及分子信息进行空间定位和检测。
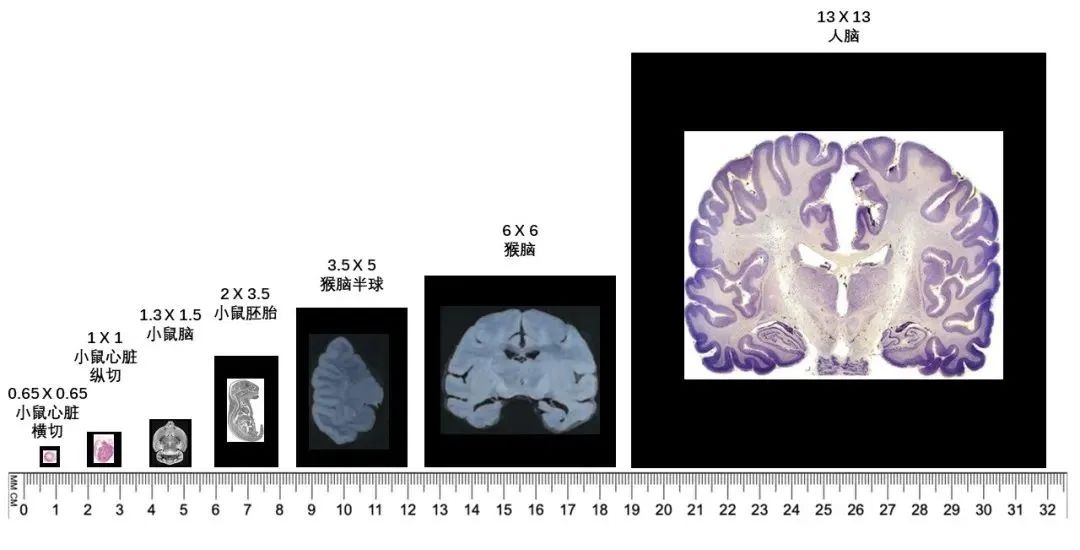
02 厘米级全景视场,检测组织大小可定制
Stereo-seq设计的常规芯片大小为1 cm×1 cm,同时可依据组织大小定制不同尺寸的芯片。华大时空组学现已推出时空芯片S0.5,该芯片尺寸为0.5 cm×0.5 cm,可灵活兼容现有技术流程,极大地提升芯片利用率,同时依旧可以实现高水平的细胞分割。未来,华大时空组学还将根据实际科研需求推出大尺寸芯片。
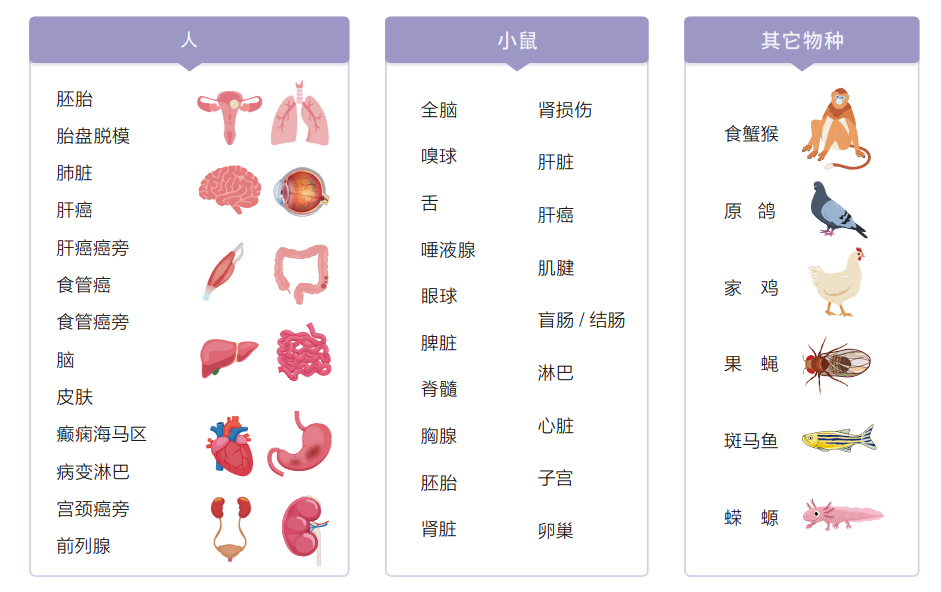
03 物种组织不设限,人、动物及植物多覆盖
Stereo-seq技术目前已研发了针对人、不同动物及植物的各部位组织器官的检测方法,完成了多种动植物的组织器官研究。
04 自主研发时空云平台STOmics Cloud,加速科研转化
Stereo-seq配套搭建了领先的多组学数据分析平台时空云平台STOmics Cloud,支持用户在线进行时空组学数据挖掘和分析结果可视化,全链助力时空科研成果产出。
同时,时空云平台STOmics Cloud基于大语言模型,创新建立了人工智能应用StereoCopilot,可以灵活辅助研究人员进行科研设计、数据分析及文章撰写等。
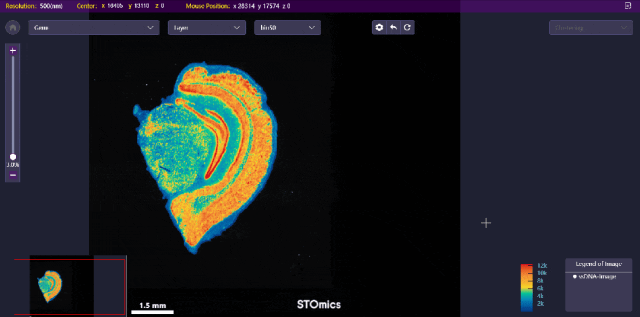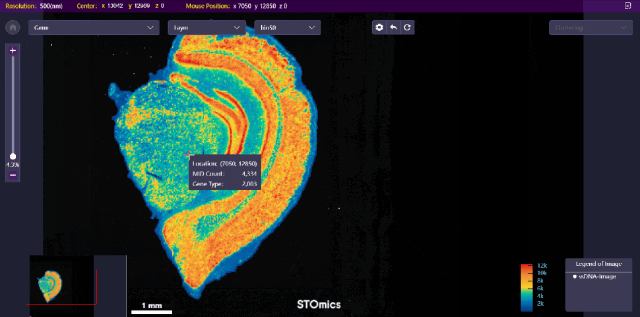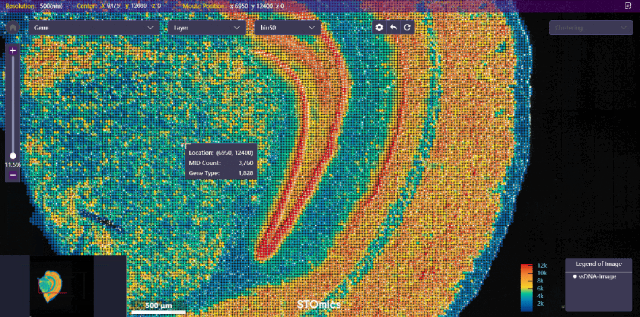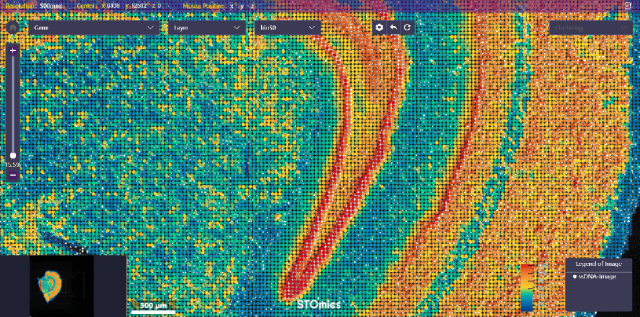
小鼠大脑演示数据
关于贝瑞基因
北京贝瑞和康生物技术有限公司(简称贝瑞基因)成立于2010年5月,是致力于应用高通量基因测序技术,为生命科学研究和临床医学疾病筛查提供整体解决方案的研发型高新技术企业。从2012年至今,贝瑞基因一直荣获"国家高新技术企业"认证,并于2017年8月成功登陆A股主板上市。
贝瑞基因与全球测序平台供应商一直保持高度紧密的战略合作,拥有多台国际主流的高通量测序平台和单细胞平台。贝瑞基因依托于公司强大的高通量测序平台和生物信息分析资源,开发了几十种产品,覆盖了基因组、转录组、单细胞等科研服务类型,搭建了成熟的生产、分析、项目管理、售前售后服务流程,致力于为科研人员提供前沿、完善的基因组学解决方案。截止目前,贝瑞基因已为国内、国际科研工作者提供了65余万份科研样本的文库构建及测序分析工作。在单细胞转录组、空间组学方面,贝瑞基因积累了大量项目经验,累计处理1W+例样本,涵盖500+种组织类型。目前,贝瑞基因支持单细胞用户发表多篇Nature、Cell、Immunity、Nature Cell Biology、Cell Research、Journal of Hepatology、Gut、Protein&Cell、Theranostics、PNAS 等期刊文章,影响因子累积高达880+。
关于华大时空
华大作为时空组学领域的重要推动者,在2020年发布了自主研发的时空组学技术Stereo-seq,华大时空组学STOmics应运而生,助力生老病死、意识起源、万物生长、生命起源等重大科学问题的研究与应用。
2022年,凭借能同时实现“纳米级分辨率”和“厘米级全景视场”的技术优势,Stereo-seq助力研究人员陆续在Cell、Nature和Science三大顶级学术期刊发表胚胎发育、器官再生、疾病等领域的重要成果。
秉承华大集团“基因科技造福人类”的使命,华大时空组学STOmics将积极推进全球科研合作,同时致力于促进时空组学技术的产业化应用,为科研和临床领域带来新的认知及价值。
参考文献:
Chen A, Liao S, Cheng M, et al. Spatiotemporal transcriptomic atlas of mouse organogenesis using DNA nanoball-patterned arrays[J].Cell, 2022,185(10):1777-1792.e21. doi:10.1016/j.cell.2022.04.003.