深圳华大生命科学研究院联合复旦大学附属中山医院等单位,利用华大自主研发的时空组学技术Stereo-seq,系统地测试了临床样本制备过程对时空组学结果产生的影响。文章通过临床图像与时空分子信息结合分析,为众多时空组学项目的顺利开展,在样本的有效前处理、临床组织实验方案选择等方面,提供了及时、可靠、系统的解决方案。该成果于2022年1月26日发表于Clinical and Translational Medicine,下面是文章共同第一作者姜宇佳老师的详细解读。

文章题目:Clinical challenges of tissue preparation for spatial transcriptome
发表时间:2022-01-26
发表期刊:Clinical and Translational Medicine
主要研究团队:深圳华大生命科学研究院、复旦大学附属中山医院等
影响因子:11.492
DOI:10.1002/ctm2.669
研究背景
随着生物技术的不断发展,传统医学正在从分子医学向时空分子病理学发展。后者是指,在时间和空间维度上,将临床表型与分子信息结合,利用医学、跨组学和生物信息学等交叉学科,形成包含时空转录组学、蛋白质组学、代谢组学等生物学信号的数字病理信息,为患者开展病灶定位、分子靶向和动力学监测的诊断与治疗。
缺少有效的时空信息测量和分析方法,限制了时空分子医学临床应用。近年发展起来的时空组学,有望为此提供关键的解决方案。时空组学通过带有标签的核酸探针,杂交捕获组织切片中的mRNA,高通量测序,最终分析还原mRNA空间位置信息,从而构建组织原位的空间转录图谱。可以原位表征新细胞簇、细胞与细胞间相互作用。时空转录组信息与临床图像对应后,可以进一步研究病理表型和分子信息之间的关系,高分辨率揭示人体组织的细胞异质性和转录组变化。
当前,时空组学临床应用的挑战是,对其实际价值和重要性、临床组织制备及其数据分析和指征仍缺乏足够的理解。因此,针对时空转录组数据的产出,确定临床实践中样本制备和保存的合适条件,建立有效的质控,是临床组织的高效制备、时空数据的高质量获取的关键环节,也是将临床病理图像和时空分子信息结合进行临床实践的关键步骤之一。
本研究利用Stereo-seq技术,系统地测试并分析了临床样本从获取到测序环节中各关键步骤对时空组学数据产出和分析结果的影响。这些关键步骤,包括样本选择、手术方式、样本收集、保存、运输、加工、储存、质控和测序环节等。
研究样本
57对肺癌、癌旁组织或正常组织,共125个样本,其中分析研究阶段采集了33对组织共77个样本,验证研究阶段采集了24对组织共48个样本。
研究策略
对不同条件收集到的样本进行组织学评分(histologicals cores)、RNA完整性(RNA integrity number,RIN)评分和Stereo-seq测序,并对评分结果进行统计分析(图1)。
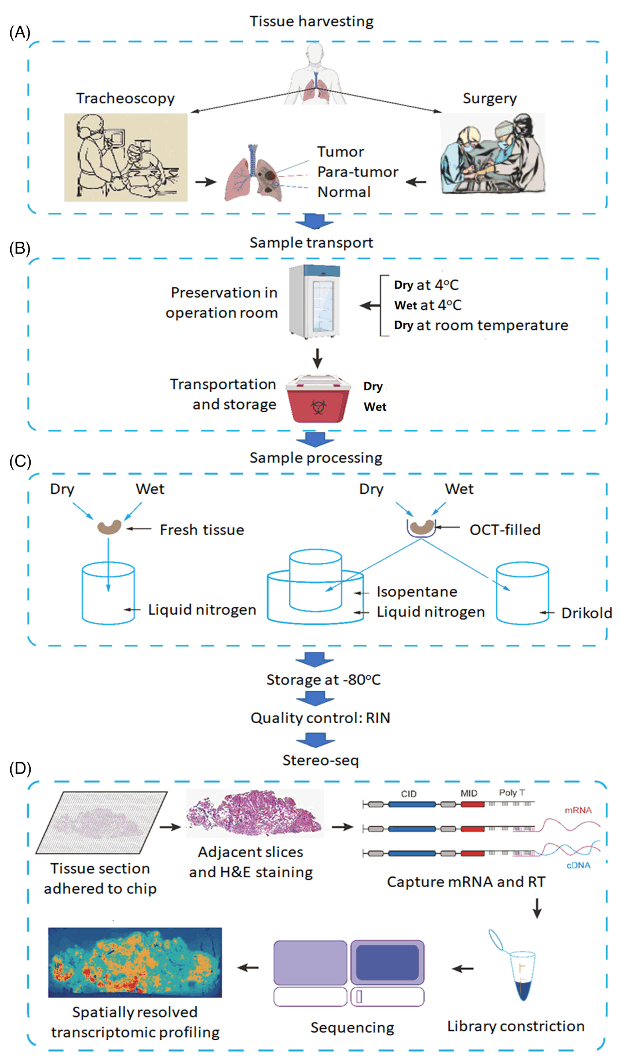
图1 实验及分析流程
研究成果
1. 样本H&E染色和RIN值的评分
首先,研究团队中的病理医生详细地统计了患者的病理特征,包括性别、年龄、癌症家族史、既往癌症史、吸烟史、病理类型、T分类、淋巴转移阶段和肿瘤淋巴结转移(tumour-node-metastasis,TNM)阶段。然后,将不同病理特征的组织进行H&E和RIN值评分(图2)。RIN值主要为<6、=6~7和>7等三类;H&E评分主要为<90、≥90两类。
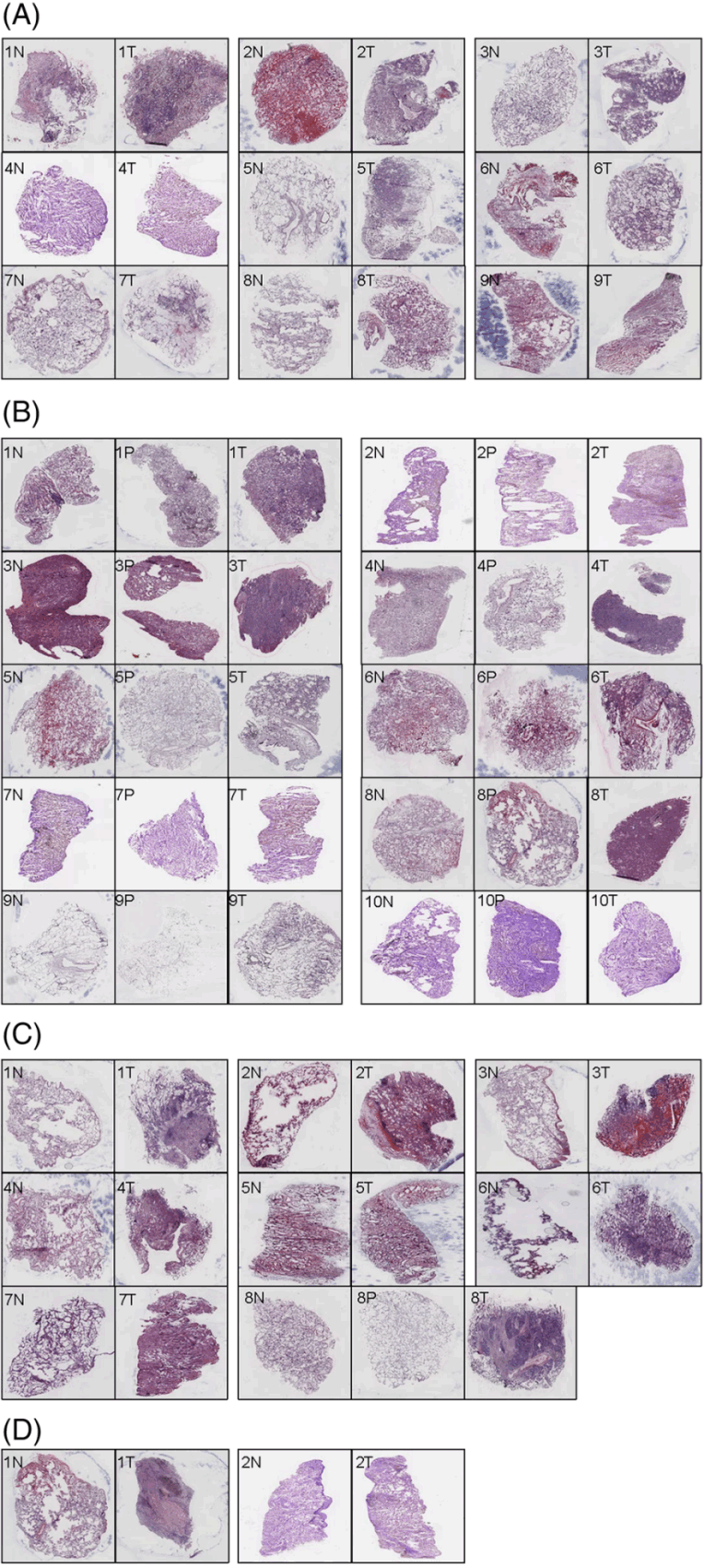
图2 不同类型肺癌配对样本(正常组织、肿瘤组织或癌旁组织)的H&E红染色图像
2. 确定样本制备的关键步骤
根据病理医生临床样本采集建议和时空组学实验经验,确定了样本制备及储存的7个关键环节及条件:组织类型、取样方式、手术室保存时间、运输条件、样本前处理方式、包埋方式、-80℃下存储天数(图3)。
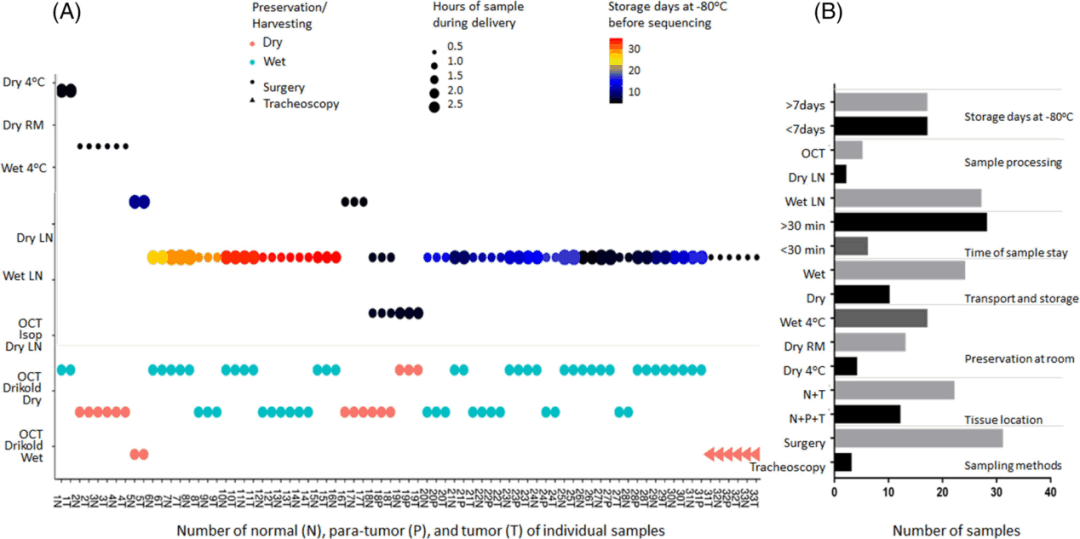
图3 每个样本统计及处理的信息
3. H&E染色评分、RIN值评分与制备步骤的关系
将H&E和RIN值评分与关键步骤进行统计分析,结果发现:正常组织和肿瘤组织之间的H&E评分存在显著差异(P<0.01,图4A),正常组织和肿瘤组织之间,正常组织、癌旁组织和肿瘤组织之间RIN值评分存在显著差异(P<0.01),而癌旁组织和肿瘤组织之间的H&E评分无统计学差异(图4C、4D);湿处理组织的H&E评分和RIN值评分水平显著低于干处理组织(P<0.01、P<0.05;图4E、4F);离体时间超过30min的组织的H&E评分低于≤30min的组织的评分,而二者的RIN值评分无统计学差异(图4G、4H)。液氮中干组织和OCT(optimal cutting temperature compound)浸润组织的H&E评分和RIN值评分,高于液氮中的湿组织(图4I、4J)。在-80℃下储存超过7d的组织中的H&E评分低于储存≤7d,而RIN评分不存在此现象(图4K、4L)。H&E评分和RIN值评分的相关系数为0.63,具有显著性(P<0.01,图4M)。
综上,通过对不同样本的H&E和RIN值评分的统计结果进行分析,可以发现,不同的处理方案之间存在差异,例如干燥处理方案好于湿处理方案,离体时间小于30 min方案好于超过30 min等。且组织细胞层面的H&E评分和分子层面的RIN值评分之间,存在不同水平质控效果的差异,例如,癌旁组织和肿瘤组织之间的H&E评分无显著差异,但RIN评分却有显著差异。这说明,仅通过传统的质控方案,无法精准地对样本进行质量评估,需进一步探索结合所产出空间转录组学数据质控反馈,来明确样本制备的质控标准。
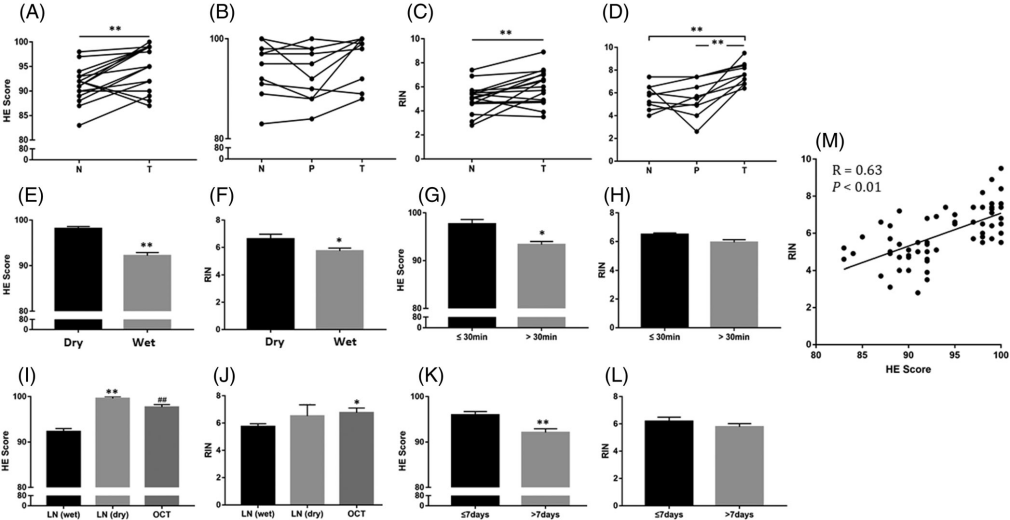
图4 样本采集和处理中HE和RIN评分的影响因素
4. Stereo-seq测序结果与制备步骤的关系
为了进一步揭示不同变量与Stereo-seq的数据质量之间的关系。研究人员提出了bin50-UMI/饱和度/测序总读数(BUSSTR)概念,即在相同测序深度、相同bin50捕获面积下可以成功捕获的UMI数量。随后统计了每一个样本的BUSSTR值,并进行了比较,结果显示:肿瘤样本的BUSSTR水平高于正常组织(图5B),干样品BUSSTR高于湿样品(图5D),样本离体时间≤30min明显高于>30 min(P<0.05,图5E)。
气管镜检查和手术方法之间无统计学差异(图5C),-80℃条件下的保存天数≤7d与>7d也无统计学差异(图5G),同样,干湿组织在液氮和OCT中的储存条件也没有统计学差异(图5F)。RIN值评分、H&E评分与UMI之间无统计学相干性(图5H、5I)。分RIN< 6、RIN= 6 ~ 7或RIN> 7三组进行差异分析,发现与UMI之间也无统计学差异(图5J)。
以上结果可以看出,在样本的处理过程中存在两个核心关键步骤:样本离体时间小于30 min和样本干燥处理方案。相比于其他环节,这两个步骤与最终的测序结果质量存在更加显著的相关性。
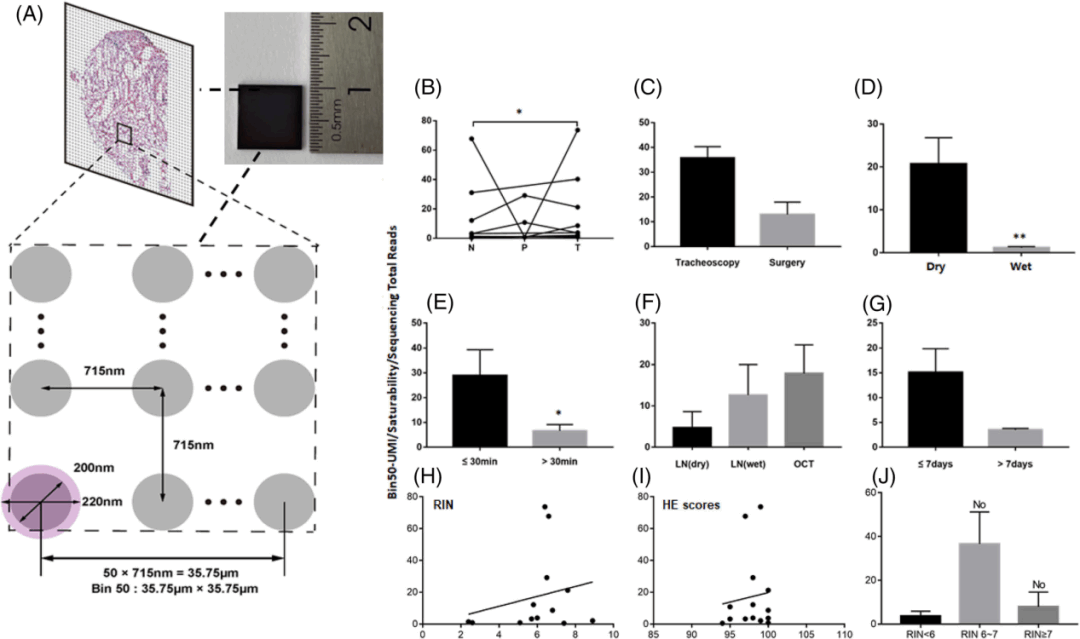
图5 空间转录组数据的质量控制
5. 比较不同制备步骤的Stereo-seq数据质控结果
经过以上研究分析,确定了“样本离体小于30min内处理”和“干燥处理条件”两个与测序结果显著相关的步骤。为了进一步表征这两步骤与Stereo-seq结果的关系,研究人员通过Stereo-seq的可视化分析,对不同影响因素进行了相关质控分析。结果发现,满足“样本离体小于30min内处理”和“干燥处理条件”的组织(图6C、6D),捕获基因数和UMI数更高,降维聚类效果更好,可以满足后续的分析要求(图6S、6T)。
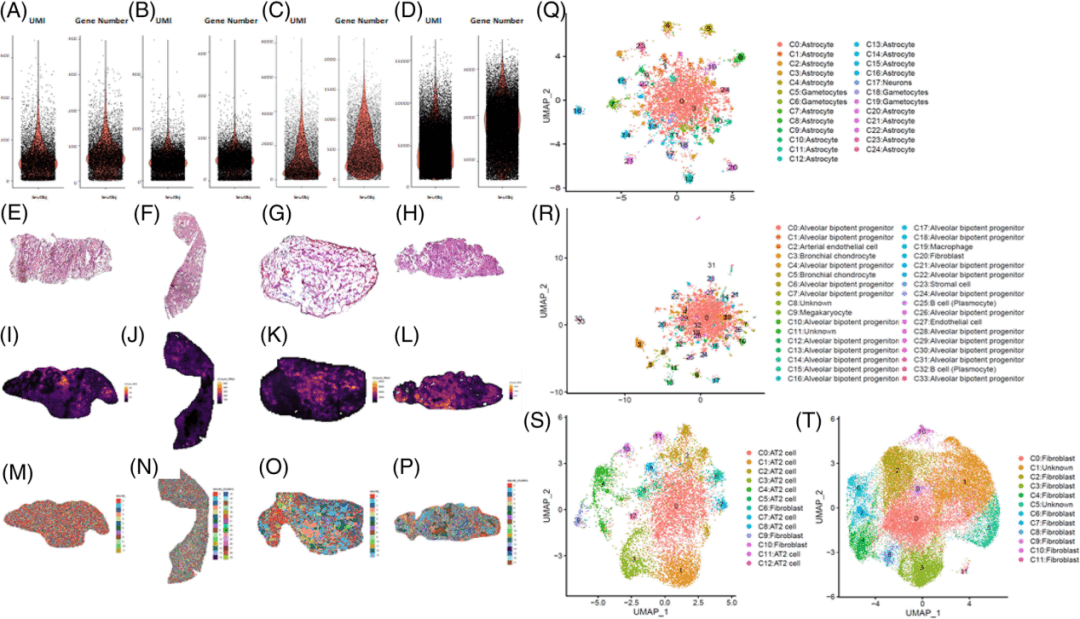
图6 空间转录组学质量控制的可视化图像
总结
时空组学逐渐成为人类疾病研究的重要技术手段,预期可以更加高效、广泛地应用于人类临床疾病研究,为人类疾病的诊断、治疗及预防提供新的方案。时空组学研究中临床样本的选择,高度依赖于临床医生对病理特征和病变程度的理解。可通过后者给出的组织病理学诊断和局部病变确认,来选择用于时空组学研究获取数据信息的可用性。临床样本的处理和存储条件,会对时空组学数据质量产生较大影响。
本研究通过将不同样本处理条件与组织学评分、RIN值评分和Stereo-seq测序结果进行关联分析,明确了影响最终测序质量的两个关键前处理环节(手术室保存时间和样本前处理),并给出具体操作建议:样本离体后30 min内尽快进行处理、对样本进行干燥处理。这样临床样本制备成功率高,且获得的时空组学数据质量高,值得应用时空组学开展基础研究和临床转化医学研究借鉴。
作者: 姜宇佳







